 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站! 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站!肝细胞癌进展
肝纤维化/肝硬化相关的 ECM 沉积会显著提高基质刚度(matrix stiffness),而“刚度如何被肿瘤细胞感知并转译为促癌转录程序”,尤其是与表观调控和代谢重编程之间的直接桥梁,仍缺乏清晰的因果链条。作者把这个“桥梁”定位到了 YEATS2(ATAC 复合体关键组分、乙酰化修饰 reader)。
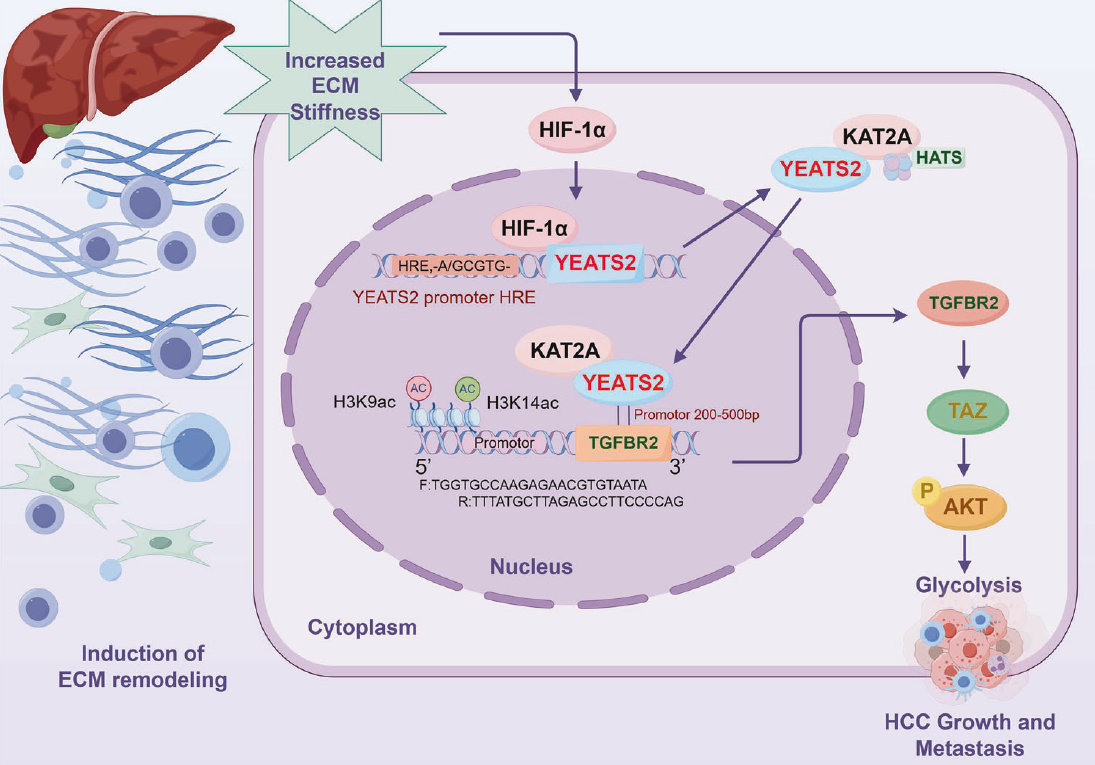
基质刚度↑ 通过 HIF-1α 上调 YEATS2;YEATS2 招募 KAT2A 增强 TGFBR2 启动子 H3K9ac/H3K14ac,表观激活 TGFBR2 转录,进而驱动 p-SMAD2/3→TAZ→AKT 轴与糖酵解增强,促进 HCC 增殖、EMT 与转移。
结论 1:YEATS2 在 HCC 中上调,并与不良临床特征及更差生存相关
作者用多套 GEO/TCGA 数据集与自建队列(63 对配对样本)验证 YEATS2 在肿瘤组织显著升高;并显示 YEATS2 高表达与肝硬化、肿瘤多灶、微血管侵犯等临床特征相关,同时 OS/DFS 更差。
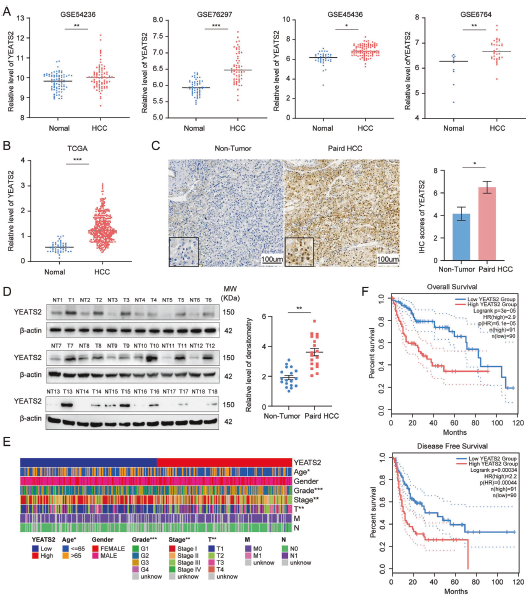
Fig1. YEATS2 在肝癌组织中高表达,并与患者不良预后相关
结论 2:YEATS2 促进 HCC 细胞增殖、迁移/侵袭与 EMT;敲低可抑制体内生长与转移
体外:YEATS2 敲低降低活力/增殖/克隆形成,抑制 Transwell 迁移侵袭,并使 EMT 与基质降解相关蛋白(如 vimentin、N-cadherin、MMP2/9)下调、E-cadherin 上调;过表达则相反。
体内:在皮下成瘤、尾静脉肺转移、脾内注射肝转移模型中,YEATS2 敲低均显著降低肿瘤生长与转移灶负担,并在瘤组织层面对应降低增殖/EMT/转移相关标志。
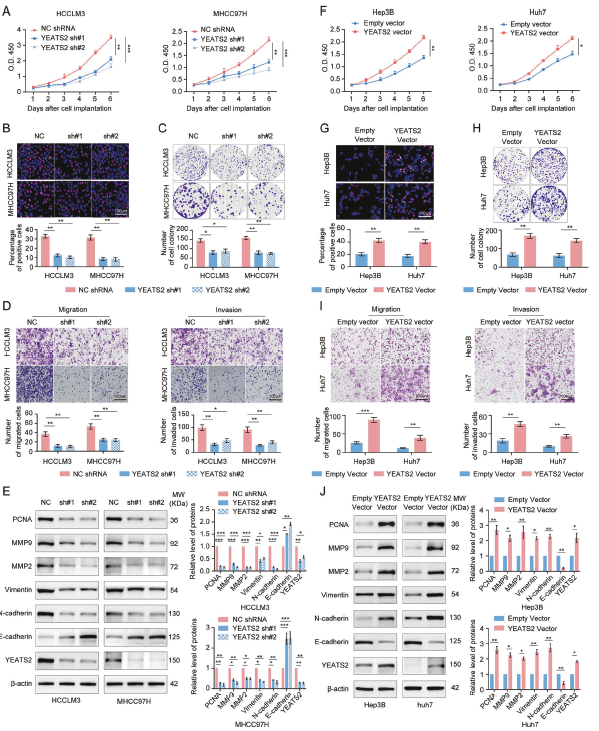
Fig2. YEATS2 在体外促进肝细胞癌细胞的增殖、转移及 EMT
结论 3:YEATS2 通过“表观激活 TGFBR2→SMAD2/3→TAZ→AKT”驱动糖酵解重编程与促癌表型
3.1 YEATS2 激活 TAZ/AKT 并增强糖酵解
RNA-seq + 蛋白质组提示代谢、PI3K-AKT、Hippo 相关富集;功能上 YEATS2 上调会增加葡萄糖摄取与乳酸产生,并提高多种糖酵解酶表达;分子上 YEATS2 上调 TAZ 蛋白与 AKT Ser473 磷酸化(对 YAP1 影响不明显),并且 TAZ 敲低可压低 p-AKT,提示 TAZ 位于 AKT 上游。药理抑制(Verteporfin、MK-2206)可削弱 YEATS2 的代谢表型。
3.2 TGFBR2 是 YEATS2 的关键下游靶点;而 YEATS2 通过招募 KAT2A 在 TGFBR2 启动子做 H3K9ac/H3K14ac 来“开机”
锁定靶点:RNA-seq 与 TMT 蛋白组交集优先命中 TGFBR2;在功能上,TGFBR2 敲低可逆转 YEATS2 过表达带来的糖酵解增强、增殖/侵袭增强,并下调 TAZ 与 p-AKT。YEATS2 还增强 p-SMAD2/3,而 TGFBR2 敲低或 SMAD2/3 磷酸化抑制剂(SB431542)可阻断 YEATS2-TGFBR2 轴对 TAZ/p-AKT 的驱动。
表观机制:YEATS2 本身无 HAT 活性,但其过表达选择性提高全局 H3K9ac/H3K14ac;ChIP-qPCR 显示 YEATS2 结合并增强 TGFBR2 启动子特定区段的 H3K9ac/H3K14ac。筛选与 Co-IP 证明 YEATS2 与 KAT2A 互作,且 KAT2A 负责在该启动子位点的乙酰化沉积;KAT2A 敲低可消除 YEATS2 诱导的启动子乙酰化与 TGFBR2 上调。
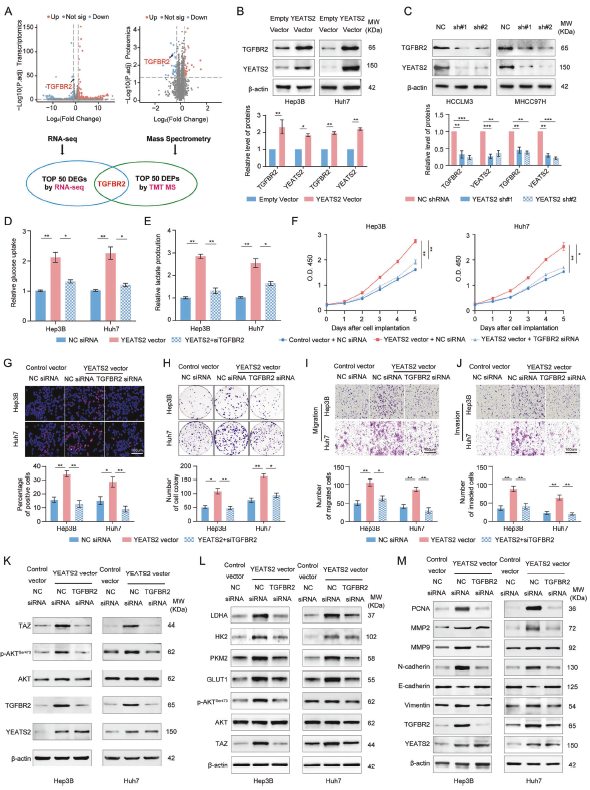
Fig3. TGFBR2 介导 YEATS2 在肝细胞癌细胞中驱动的增殖、转移及糖酵解增强效应
结论 4:基质刚度通过 HIF-1α 上调 YEATS2,且 YEATS2 是刚度促癌效应的关键中介
作者用不同刚度的聚丙烯酰胺水凝胶(软 vs 硬)培养 HCC 细胞,发现硬基质可提高 YEATS2、H3K9ac/H3K14ac、并伴随 HIF-1α 上升;敲低 HIF-1α(而非 p300)可阻断“刚度→YEATS2↑”及相关表观改变。进一步 ChIP-qPCR 指向:刚度增强 HIF-1α 在 YEATS2 启动子 HRE 的结合。功能上,硬基质诱导的糖酵解增强、增殖与 EMT/侵袭相关表型,可被 YEATS2 敲低(或糖酵解抑制 2-DG)显著削弱。终模型图总结为:stiffness→HIF-1α→YEATS2→KAT2A→TGFBR2→TAZ/AKT→glycolysis→HCC progression。
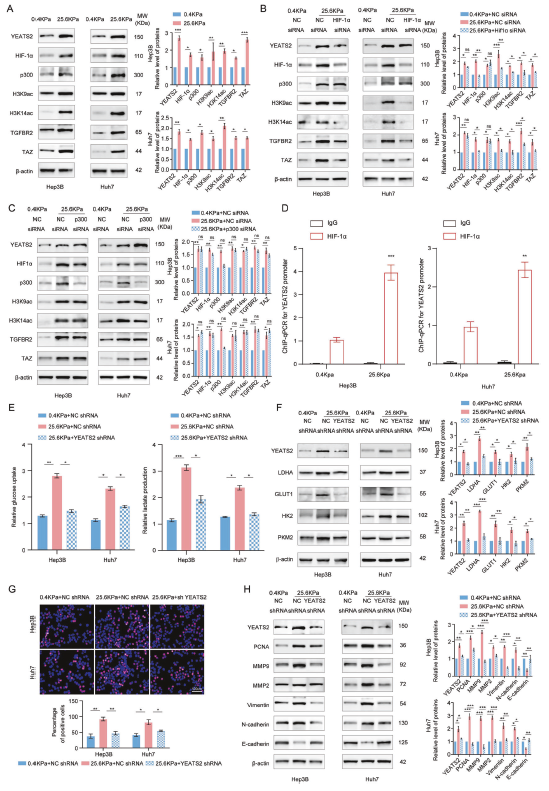
Fig. 4 基质刚度通过 HIF-1α 上调 YEATS2,并促进其致癌效应
研究逻辑总结:
1)先研究临床相关性:YEATS2 上调 + 预后/侵袭性特征关联。
2)再验证功能必要性:体外增殖/侵袭与体内生长/转移模型证明 YEATS2 促癌。
3)随后检测下游通路闭环:YEATS2→(TGFBR2/p-SMAD2/3)→TAZ→AKT→糖酵解→表型,并用 siRNA + 抑制剂做路径定位。
4)然后表观分子机制:YEATS2 招募 KAT2A,在 TGFBR2 启动子沉积 H3K9ac/H3K14ac 解释“YEATS2 无酶活也能上调靶基因”。
5)上游微环境输入:基质刚度通过 HIF-1α 转录性上调 YEATS2,把“力学信号→表观→代谢→肿瘤进展”串成一条链。