 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站! 欢迎来到乐鱼网页版登录入口网站!
欢迎来到乐鱼网页版登录入口网站!
Ø 研究背景
脓毒症是重症监护室患者死亡的主要原因,其中高达60%的患者会出现脓毒症诱导的心肌病(SICM),表现为射血分数降低、左心室扩张和早期可逆性心肌功能障碍。SICM显著影响脓毒症患者的预后和死亡率,其死亡率约为无心肌功能障碍脓毒症患者的三倍。心脏免疫稳态在逆转心肌功能障碍和促进心脏康复中发挥关键作用,巨噬细胞是脓毒症心脏中主要的免疫细胞。规律运动可减轻代谢和免疫适应不良,保护心血管,但运动如何调节心脏免疫微环境尚不清楚。因此,本研究旨在探讨自愿跑步是否通过预训练心脏巨噬细胞来保护脓毒症诱导的心肌病中的心脏功能。
Ø 研究结果
2.1 规律运动通过调节心脏免疫微环境保护SICM心脏功能
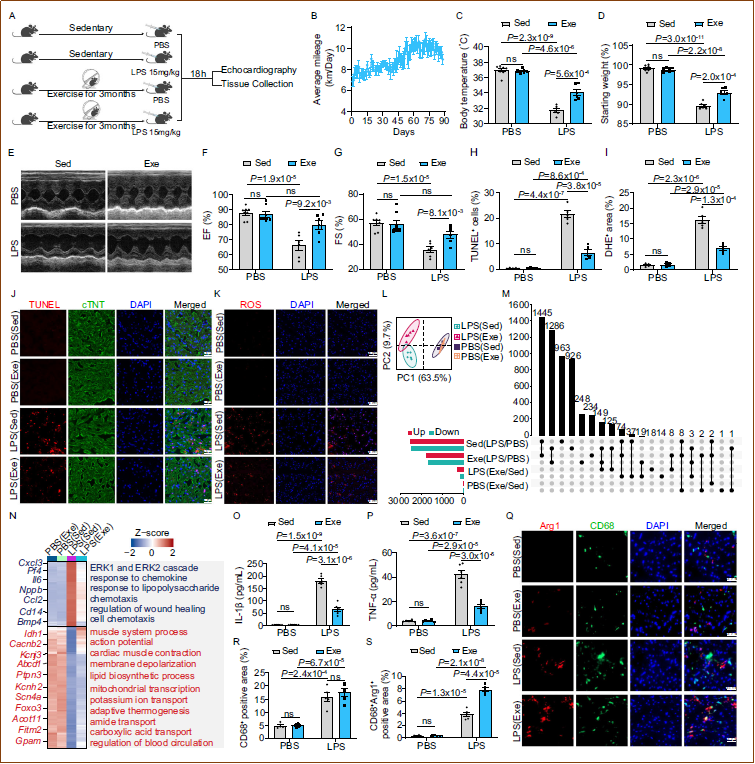
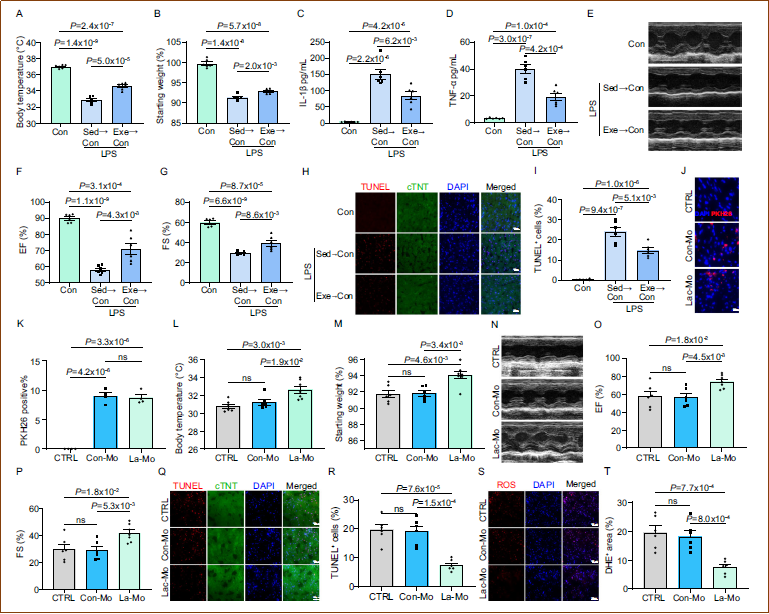
研究人员让小鼠进行三个月的自愿跑步训练,随后通过腹腔注射脂多糖(LPS)诱导脓毒症。结果显示,规律运动显著保护小鼠免受LPS诱导的脓毒症伤害,表现为体温下降和体重减轻程度降低。超声心动图显示,运动组小鼠的射血分数(EF)和短轴缩短率(FS)分别改善了约21%和34%。TUNEL和DHE染色显示运动减少了心肌细胞凋亡和氧化损伤。Bulk RNA测序分析表明,运动在SICM组中诱导了更显著的转录组变化,抑制了炎症相关基因(如Cxcl3、Il6、Ccl2、Cd14),激活了心脏功能相关基因(如动作电位、心肌收缩、脂质生物合成过程)。血清ELISA检测显示运动有效减轻了LPS诱导的促炎反应(IL-1β和TNF-α降低)。虽然总CD68+巨噬细胞浸润无变化,但运动使Arg1+修复型巨噬细胞增加了104%。这些结果表明,规律运动通过调节心脏免疫微环境来保护脓毒症期间的心脏功能。
2.2 自愿跑步调控脓毒症心脏免疫微环境
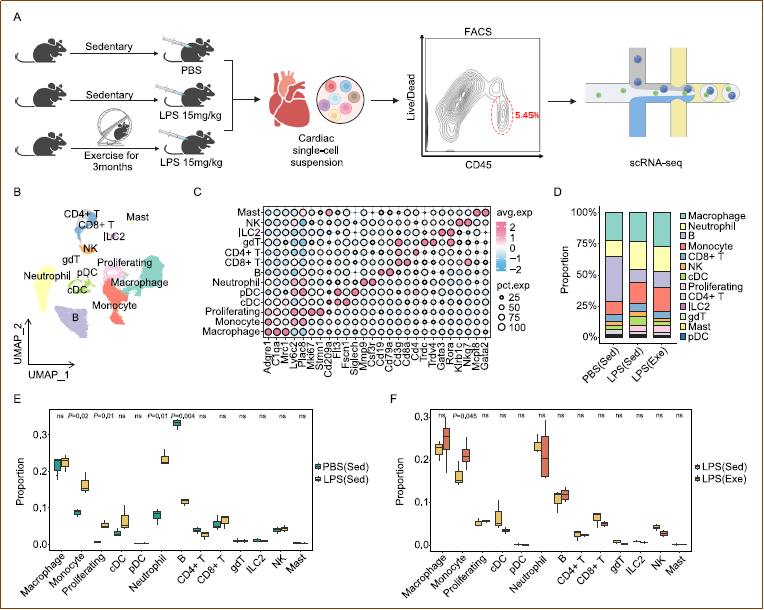
为深入表征运动对脓毒症心脏免疫微环境的影响,研究人员对PBS(久坐)、LPS(久坐)和LPS(运动)三组小鼠的心脏CD45+细胞进行了单细胞RNA测序。共获得50471个高质量细胞,鉴定出13个心脏免疫细胞群,包括巨噬细胞、单核细胞、常规树突状细胞、浆细胞样树突状细胞、中性粒细胞、NK细胞、CD4+和CD8+T细胞、γδT细胞、B细胞、ILC2型细胞、肥大细胞和增殖细胞。分析显示,脓毒症诱导了单核细胞和中性粒细胞向心脏的浸润,而规律运动显著增强了单核细胞向脓毒症心脏的浸润。Bulk RNA测序的免疫浸润分析与此一致,且PBS(久坐)和PBS(运动)组之间无显著差异。这些数据提示,规律运动通过调节单核细胞来源的巨噬细胞来调控脓毒症心脏免疫微环境。
2.3 自愿跑步调节SICM中的心脏单核细胞和巨噬细胞亚群
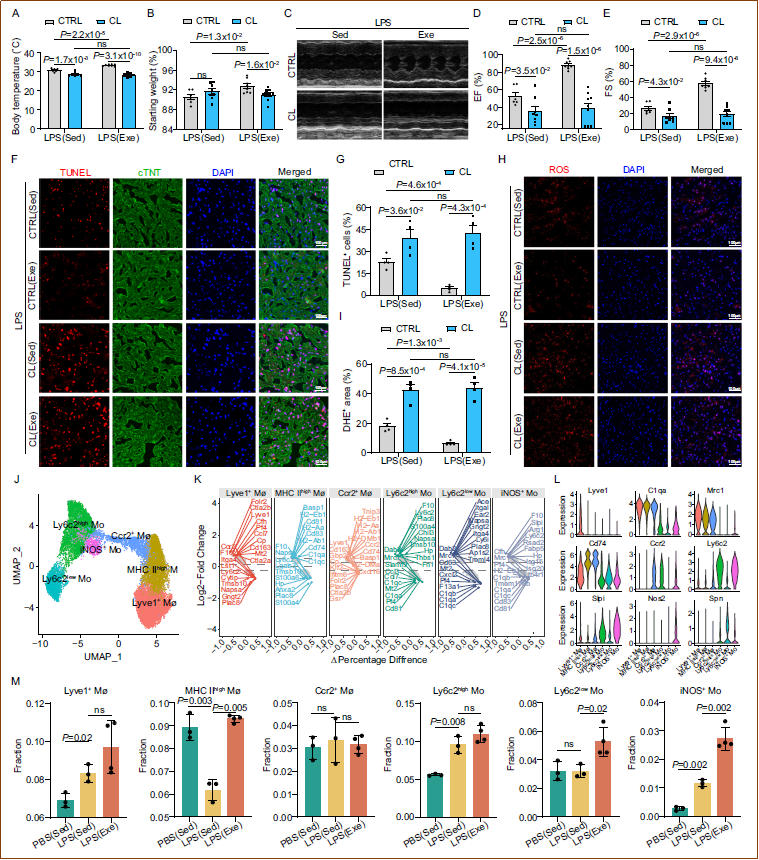
鉴于单核细胞和巨噬细胞占脓毒症心脏免疫细胞的近一半,研究人员重点研究了这些群体。通过氯膦酸盐脂质体清除单核细胞和巨噬细胞后,运动对脓毒症的保护作用(体温、体重、心脏功能、凋亡和氧化损伤的改善)被消除,表明这些细胞对运动诱导的心脏保护至关重要。二次聚类分析鉴定出六个亚群:Ly6c2低表达单核细胞、Ly6c2高表达单核细胞、Lyve1+巨噬细胞、MHC II高表达巨噬细胞、Ccr2+巨噬细胞和iNOS+单核细胞。其中,iNOS+单核细胞亚群同时表达促炎基因(如Nos2)和修复性基因(如Arg1、Slpi、Fabp5),在脓毒症心脏中显著升高且被运动进一步诱导。伪时间分析显示Ly6c2高表达单核细胞位于轨迹起始端,而MHC II高表达巨噬细胞和iNOS+单核细胞位于末端。运动还逆转了脓毒症诱导的MHC II高表达巨噬细胞减少。细胞间通讯分析揭示了运动如何调节脓毒症心脏中免疫细胞的相互作用。这些发现表明,规律运动通过调节单核细胞和巨噬细胞亚群的分化和组成来保护SICM心脏功能。
2.4 规律运动诱导单核细胞来源的iNOS+亚群保护脓毒症心脏功能
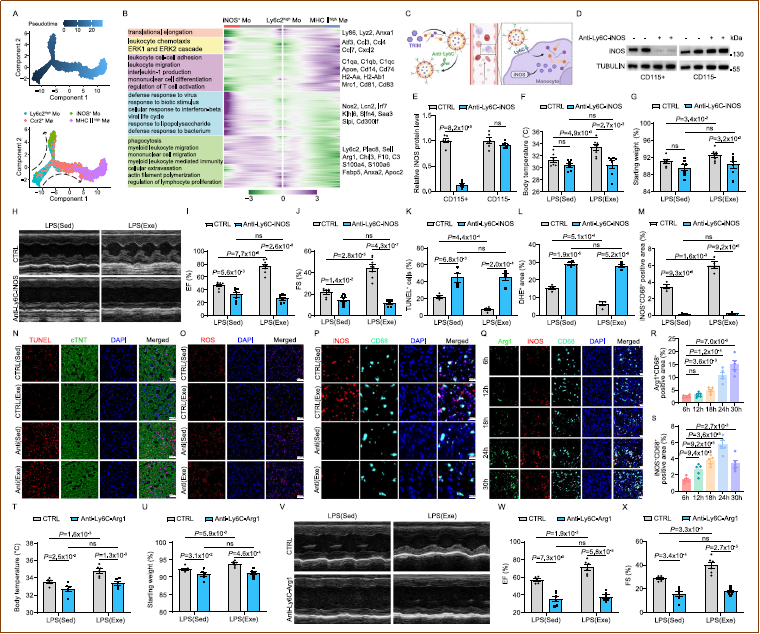
考虑到MHC II高表达巨噬细胞和Ccr2+巨噬细胞的补充或部分依赖于Ly6c2高表达单核细胞的分化,研究人员进一步探究了iNOS+单核细胞的作用。他们设计了靶向纳米抑制剂(TRIM负载的脂质体,表面偶联抗Ly6C抗体)特异性抑制单核细胞中的iNOS。结果显示,抑制iNOS消除了运动对脓毒症的保护作用,甚至在久坐小鼠中加重了LPS诱导的心脏功能障碍。时程分析显示,脓毒症期间心脏巨噬细胞从iNOS+向Arg1+转变,而运动加速了这一转变。进一步使用纳米抑制剂靶向抑制Arg1,同样消除了运动的保护效果,包括体温下降、体重减轻、IL-1β和TNF-α水平以及心肌损伤的改善,并破坏了iNOS+向Arg1+巨噬细胞的加速转变。这些发现表明,iNOS和Arg1在单核细胞来源的巨噬细胞中的表达均有助于保护SICM心脏功能,且运动加速了从iNOS+向Arg1+巨噬细胞的转变。
2.5 运动增强SICM期间单核细胞来源巨噬细胞的糖酵解和随后的组蛋白乳酸化
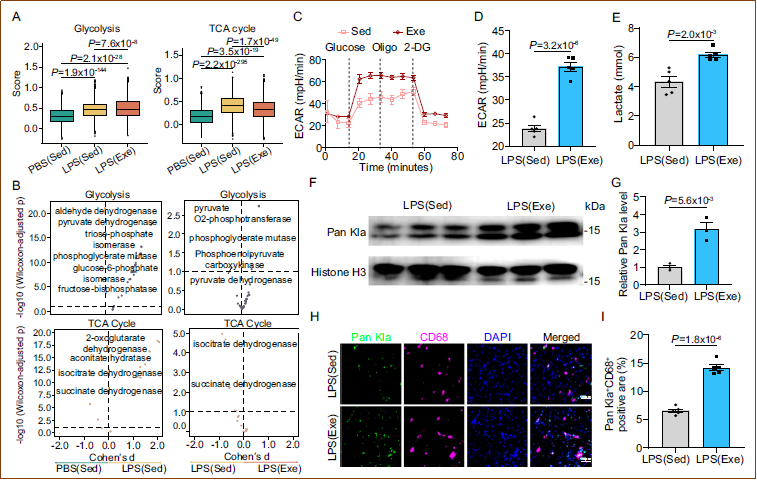
为阐明iNOS+单核细胞发挥抗炎功能的机制,研究人员分析了其代谢特征。使用Compass算法进行通量平衡分析显示,运动通过促进或抑制多种代谢通路重塑了脓毒症心脏中的巨噬细胞代谢。分析揭示,运动显著增强了整个单核细胞和巨噬细胞群体、单核细胞、巨噬细胞和iNOS+单核细胞的糖酵解,同时抑制了TCA循环。Seahorse实验验证了运动组单核细胞的糖酵解率比久坐组高约55%,细胞内乳酸水平也相应升高约50%。Western blot显示,运动在循环单核细胞和心脏巨噬细胞中诱导了全局性组蛋白赖氨酸乳酸化(Pan Kla)。这些发现表明,运动增强单核细胞糖酵解,导致乳酸产生增加,进而驱动单核细胞来源巨噬细胞的组蛋白乳酸化,这种代谢重编程有助于保护SICM心脏功能。
2.6 自愿跑步诱导单核细胞来源巨噬细胞的组蛋白乳酸化以保护SICM心脏功能
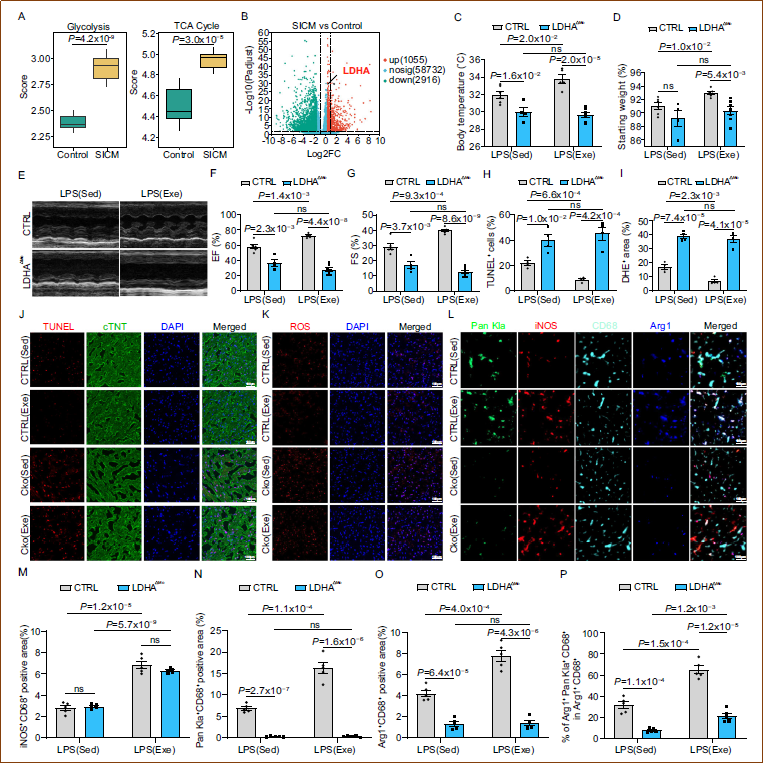
为评估这一保护机制的临床相关性,研究人员对SICM患者和健康供体的外周血单核细胞进行了RNA测序。结果显示,SICM患者单核细胞的糖酵解和TCA循环活性均增加,乳酸脱氢酶A(LDHA)表达显著升高。为探究运动诱导的组蛋白乳酸化的作用,研究人员构建了髓系细胞特异性LDHA敲除(CKO)小鼠。CKO小鼠表现出运动保护作用的逆转,包括体温下降、体重减轻、心脏功能改善以及凋亡和氧化损伤减少的效应均消失。免疫荧光分析显示,运动使心脏巨噬细胞的组蛋白乳酸化增加,且与修复标志物Arg1的表达相关,但CKO小鼠中这些增强效应均被消除。这些结果表明,运动诱导的单核细胞和单核细胞来源巨噬细胞的组蛋白乳酸化在保护SICM心脏功能中发挥关键作用。
2.7 运动增强人和小鼠单核细胞中的H3K18组蛋白乳酸化
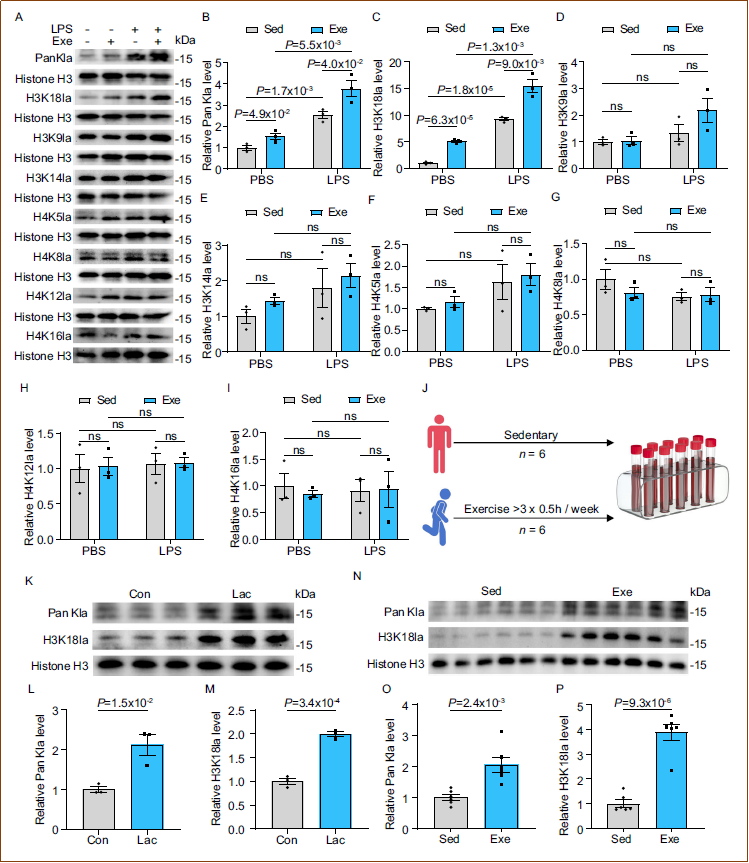
为鉴定运动诱导的组蛋白乳酸化特异性位点,研究人员检测了多种组蛋白赖氨酸残基的乳酸化水平。结果显示,H3K18la在运动后显著升高,且在LPS挑战后进一步增加,而其他位点(H3K9la、H3K14la、H4K5la、H4K8la、H4K12la、H4K16la)无显著变化。为验证运动是否在人类单核细胞中同样促进H3K18la,研究人员招募了久坐和活跃生活方式的志愿者。用20mM外源性乳酸处理久坐志愿者单核细胞后,Pan Kla和H3K18la水平增加。一致地,活跃志愿者单核细胞的Pan Kla和H3K18la水平显著高于久坐个体。时程分析显示,1天或7天运动不改变组蛋白乳酸化水平,但14天运动后显著增加,28天运动后进一步升高。14天运动即可减轻体重下降并保护心脏功能,28天运动增强这些保护效果。这些发现证明,运动诱导人和小鼠单核细胞中的H3K18la,在保护SICM心脏功能中发挥关键作用。
2.8 运动通过p300和HDAC2增强单核细胞中的H3K18组蛋白乳酸化
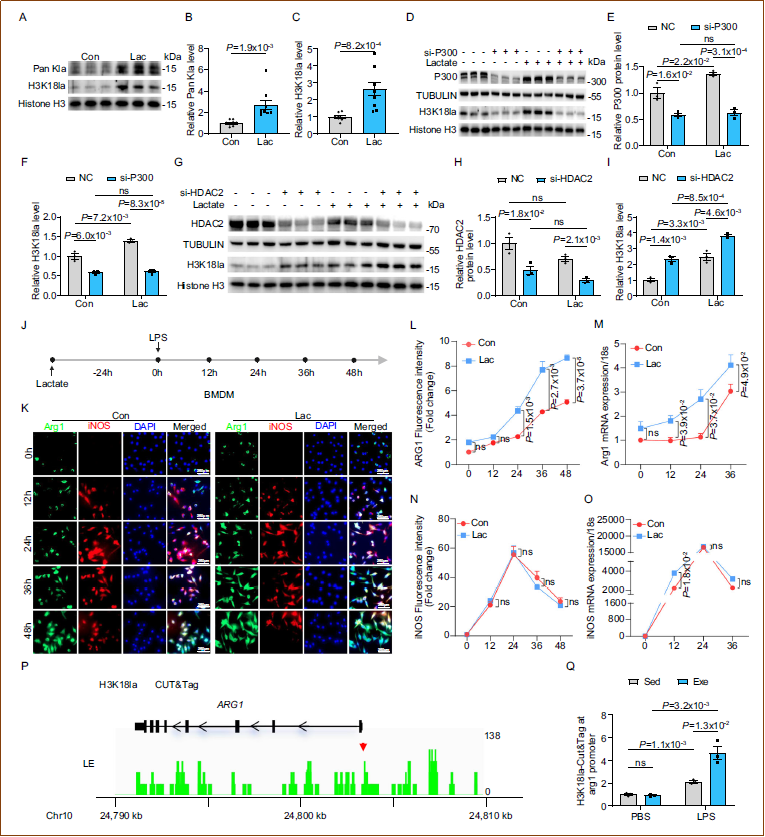
为鉴定H3K18la的乳酸转移酶和去乳酸化酶,研究人员聚焦于p300和HDAC1-3。siRNA沉默p300后,乳酸诱导的Pan Kla和H3K18la被消除,表明p300是单核细胞中H3K18la的乳酸转移酶。沉默HDAC2(而非HDAC1或HDAC3)显著增加H3K18la水平,表明HDAC2是主要的去乳酸化酶。为阐明H3K18la是否调控iNOS+向Arg1+巨噬细胞的转变,研究人员用乳酸预处理骨髓来源巨噬细胞(BMDM),然后进行LPS时程挑战。乳酸预处理显著增强Arg1表达而不影响iNOS表达,促进了向修复型巨噬细胞的更快转变。CUT&Tag分析显示H3K18la在Arg1启动子区域显著富集,且LPS刺激后富集增加,运动背景下富集程度更高。这些结果表明,运动诱导的H3K18la由p300和HDAC2调控,通过促进向修复型巨噬细胞的更快转变和恢复免疫稳态来发挥保护作用。
2.9 乳酸教育的单核细胞输注改善SICM心脏功能
,研究人员评估了这些发现的转化应用价值。在更临床相关的盲肠结扎穿孔(CLP)多微生物脓毒症模型中,运动同样显著防止了体温下降、体重减轻、IL-1β和TNF-α产生增加,改善了心脏功能,减少了凋亡和氧化应激。过继转移实验显示,将运动供体小鼠的单核细胞输注到久坐受体小鼠中,显著缓解了脓毒症引起的体温下降、体重减轻和炎症因子产生,改善了心脏功能并减少了心肌凋亡。为模拟运动的益处,研究人员用乳酸培育的循环单核细胞以诱导组蛋白乳酸化,然后输注到SICM小鼠中。PKH26标记证实这些单核细胞定位于心脏。乳酸培育的单核细胞输注显著增强了心脏功能,减少了脓毒症心脏的凋亡和氧化损伤,效果与自愿运动相似。用p300抑制剂C646预处理的单核细胞输注则消除了运动保护作用。这些发现表明,H3K18la对保护SICM心脏功能至关重要,乳酸诱导的单核细胞过继转移是一种有前景的治疗策略。
Ø 研究结论
本研究系统阐明了运动保护脓毒症诱导心肌病的分子机制:规律运动通过增强单核细胞糖酵解,增加乳酸产生,进而通过p300介导的H3K18组蛋白乳酸化和HDAC2介导的去乳酸化调控,诱导单核细胞来源巨噬细胞中修复性基因(如Arg1)的表达,促进巨噬细胞从促炎表型(iNOS+)向修复表型(Arg1+)的快速转变,从而恢复心脏免疫稳态、减轻炎症反应、减少心肌细胞凋亡和氧化损伤,终保护心脏功能。研究还鉴定了一个独特的iNOS+Arg1+巨噬细胞亚群,其同时表达促炎和修复基因,在脓毒症早期发挥清除细胞碎片的作用,随后加速炎症消退。重要的是,该研究证明了乳酸培育的单核细胞过继转移可模拟运动的保护效果,为脓毒症诱导的心肌病提供了一种潜在的细胞治疗策略。此外,活跃生活方式人群的循环单核细胞表现出更高的组蛋白乳酸化水平,提示该机制具有临床转化价值。
Sun S, Lai C, Huang C, Ren X, Zhang T, Zou J, Tong Y, Zhou Q, Lu J, Shen Z, Chen W, Wang R, Rabrenovic N, Wang X, Ma B, Qian J, Fu G, Shang M. Exercise-induced histone lactylation in monocyte-derived macrophages restores cardiac immune homeostasis and function in sepsis-induced cardiomyopathy. Nat Commun. 2025 Dec 15;17(1):756. doi: 10.1038/s41467-025-67443-8. PMID: 41398160; PMCID: PMC12819526.